سیستمی مدرن در پزشکی برای پایش میکروب های روده و ارتباط آنها با مغز
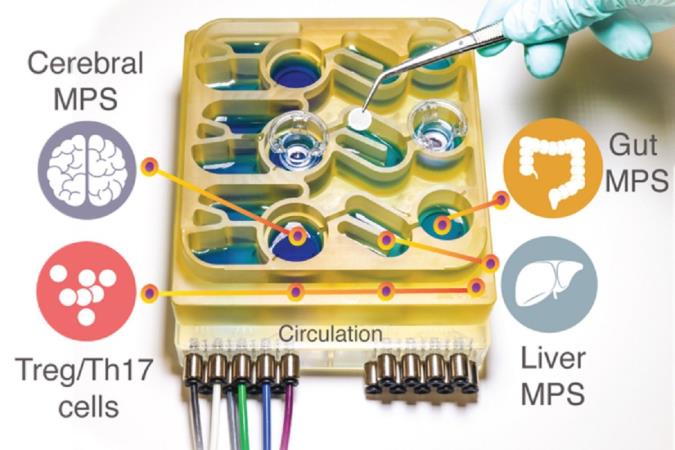
تصویر: اندام روی تراشه. محققان یک سیستم “اندام بر روی یک تراشه” ایجاد کرده اند که تعاملات بین مغز، کبد و روده بزرگ را تکرار می کند. با مجوز از محققان. عکس از مارتین تراپکار، MIT
سیستم «اندام ها بر روی یک تراشه» یا “Organs-on-a-chip” روشنایی بخش این موضوع است که چگونه باکتری ها در دستگاه گوارش انسان ممکن است بر بیماری های عصبی تأثیر داشته باشند.
از بسیاری جهات، مغز و دستگاه گوارش ما با هم ارتباط عمیقی دارند. احساس عصبی شدن ممکن است منجر به درد جسمی در معده شود، در حالی که علائم گرسنگی از روده باعث تحریک پذیری و زود رنجی ما می شود. مطالعات اخیر حتی حاکی از آن است که باکتری های ساکن روده می توانند بر برخی بیماری های عصبی تأثیر بگذارند.
از بسیاری جهات، مغز و دستگاه گوارش ما با هم ارتباط عمیقی دارند.مدل سازی این فعل و انفعالات پیچیده در حیواناتی مانند موش ها دشوار است، زیرا فیزیولوژی آنها بسیار متفاوت از انسان است. برای کمک به درک بهتر محور روده و مغز، محققان یک سیستم “اندام بر روی یک تراشه” ایجاد کرده اند که تعاملات بین مغز، کبد و روده بزرگ را تکرار می کند.
با استفاده از این سیستم، محققان توانستند تاثیری را که میکروب های ساکن روده بر بافت مغز سالم و نمونه های بافتی حاصل از بیماران مبتلا به پارکینسون دارند، مدل کنند. آنها دریافتند که اسیدهای چرب زنجیره کوتاه، که توسط میکروب های روده تولید می شوند و به مغز منتقل می شوند، می توانند تأثیرات بسیار متفاوتی بر سلول های سالم و بیمار مغز داشته باشند.
مارتین تراپکار ، فوق دکترای MIT و نویسنده اصلی مطالعه می گوید، “د ر حالی که اسیدهای چرب زنجیره کوتاه تا حد زیادی برای سلامتی انسان مفید هستند، ما مشاهده کردیم که تحت شرایط خاص می توانند برخی از آسیب های مغزی را بیش از حد افزایش دهند، که از جمله آنهاست جمع شدن نادرست پروتئین و مرگ عصبی که مربوط به بیماری پارکینسون است.”
ارتباط روده و مغز
برای چندین سال است که آزمایشگاه گریفیت در حال توسعه سیستم های میکرو فیزیولوژیک بوده است – که دستگاه های کوچکی هستند که می توان از آنها برای رشد مدل های بافتی مهندسی شده از اندام های مختلف، متصل شده توسط کانال های میکرو سیال، استفاده نمود. گریفیت می گوید، در برخی موارد، این مدل ها می توانند اطلاعاتی در مورد بیماری های انسانی، دقیق تر از اطلاعات به دست آمده از مدل های حیوانی ارائه دهند.
در مقاله ای که سال گذشته منتشر شد، گریفیت و تراپکار از یک سیستم میکرو فیزیولوژیک برای مدل سازی تعاملات بین کبد و روده بزرگ استفاده کردند. در آن مطالعه، آنها دریافتند که اسیدهای چرب زنجیره کوتاه (SCFAs) (short-chain fatty acids)، که مولکول های تولید شده توسط میکروب ها در روده هستند، می توانند التهاب خود ایمنی مرتبط با کولیت اولسراتیو را تحت شرایط خاصی بدتر کنند.SCFA ها که شامل بوتیرات، پروپیونات و استات هستند همچنین می توانند اثرات مفیدی بر روی بافت ها داشته باشند، از جمله در مورد تلرانس ایمنی افزایش یافته، و این که آنها موجد حدود 10 درصد از انرژیای هستند که ما از غذا به دست می آوریم.
به نظر می رسد که باکتری ها در حال حساسیت زدایی از سلول های پستانداران هستند تا آنها در مقابل خطرات موجود در محیط بیرونی واکنش زیادی نشان ندهند، و بنابراین توسط باکتری ها حالت التهاب در حال آرام شدن است.در مطالعه جدید، تیم MIT تصمیم گرفت مغز و سلول های ایمنی در گردش را به سیستم چند اندامی خود اضافه کند. مغز تعاملات زیادی با دستگاه گوارش دارد که این تعاملات می تواند از طریق سیستم عصبی روده یا از طریق گردش سلول های ایمنی، مواد مغذی و هورمون ها بین اندام ها، باشد.
چندین سال پیش، سارکیس مازمانیان، استاد میکرو بیولوژی درCaltech ، ارتباطی را بین SCFA و بیماری پارکینسون در موش ها کشف کرد. وی نشان داد کهSCFA ها، که به دلیل مصرف فیبر هضم نشده در روده توسط باکتری ها تولید می شوند، روند پیشرفت بیماری را افزایش می دهند، در حالی که موش هایی که در محیط عاری از میکروب رشد می کنند، رشد بیماری را کندتر می کنند.
گریفیت و تراپکار تصمیم گرفتند با استفاده از مدل میکرو فیزیولوژیک خود یافته های مازمانیان را بیشتر کاوش کنند. برای انجام این کار، آنها با آزمایشگاه Jaenisch در مؤسسه Whitehead همکاری کردند. Jaenisch قبلاً راهی را برای تبدیل سلول های فیبرو بلاست از بیماران پارکینسون به سلول های بنیادی پر توان، که سپس می توانند تحریک شوند به متمایز شدن به انواع مختلف سلول های مغزی – نورون ها، آستروسیت ها و میکروگلیا ها – توسعه داده بود.
بیش از 80 درصد موارد پارکینسون نمی توانند با جهش ژنی خاصی مرتبط باشند، اما بقیه علت ژنتیکی دارند. سلول هایی که محققان MIT برای مدل پارکینسون خود استفاده کرده اند دارای جهشی هستند که باعث تجمع پروتئینی به نام آلفا سینوکلئین می شود که به سلول های عصبی آسیب می رساند و باعث التهاب در سلول های مغزی می شود. آزمایشگاه Jaenisch همچنین سلول هایی مغزی ایجاد کرده است که این جهش را اصلاح کرده اند اما در غیر این صورت از نظر ژنتیکی یکسان هستند و به صورت سلول های بیمار شده از همان بیمار هستند.
باکتری های ساکن روده می توانند بر برخی بیماری های عصبی تأثیر بگذارند.گریفیت و تراپکار ابتدا این دو مجموعه سلول مغزی را در سیستم های میکرو فیزیولوژیک که به هیچ بافت دیگری متصل نبودند مورد مطالعه قرار دادند و دریافتند که سلول های پارکینسون التهاب بیشتری نسبت به سلول های سالم و اصلاح شده نشان می دهند. سلول های پارکینسون همچنین در توانایی شان در متابولیسم کردن لیپیدها و کلسترول نقصان هایی داشتند.
اثرات مخالف
محققان سپس سلول های مغز را به مدل های بافتی روده بزرگ و کبد متصل کردند و از کانال هایی استفاده کردند که به سلول های ایمنی و مواد مغذی از جمله SCFA اجازه می دهد بین آنها جریان یابند. آنها دریافتند که برای سلول های سالم مغز، قرار گرفتن در معرض SCFA مفید است و به بلوغ آنها کمک می کند. با این حال، هنگامی که سلول های مغزی مشتق شده از بیماران پارکینسون در معرض SCFA قرار گرفتند، اثرات مفید آن از بین رفت. در عوض، سلول ها، سطوح بالاتری از بد تا خوردگی پروتئین و مرگ سلول را تجربه کردند.
این تأثیرات حتی هنگام حذف سلول های ایمنی از سیستم مشاهده شد، و این، محققان را به این فرضیه رهنمون شد که اثرات ناشی از تغییر در متابولیسم چربی است.
Trapecar می گوید: “به نظر می رسد که اسیدهای چرب زنجیره کوتاه می توانند با تأثیر بر متابولیسم لیپیدها و نه تأثیر مستقیم بر تعداد مشخصی از سلول های ایمنی، به بیماری های تخریب کننده عصبی مرتبط شوند.” “اکنون هدف ما تلاش برای درک این موضوع است. “
همان طور که در روده بزرگ انسان انجام می شود، سلول های سد در کانال یک لایه متراکم از مخاط ترشح می کنند.محققان همچنین قصد دارند انواع دیگری از بیماری های عصبی را که ممکن است تحت تأثیر میکروبیوم روده قرار گیرند، مدل کنند. گریفیت می گوید، یافته ها از این ایده پشتیبانی می کنند که مدل های بافت انسانی می توانند اطلاعاتی را به دست آورند که مدل های حیوانی نمی توانند. وی اکنون در حال کار بر روی نسخه جدیدی از مدلی است که شامل رگ های خونی میکروبی است که انواع مختلف بافت را بهم متصل می کنند و به محققان اجازه می دهند نحوه جریان خون بین بافت ها در آنها را بررسی کنند.
گریفیت می گوید: “ما واقعاً باید به توسعه این موارد شدت دهیم، زیرا مهم است که شروع به وارد کردن ویژگی های انسانی بیشتر در مدل هایمان نماییم.” “ما توانسته ایم شروع به کسب اطلاعاتی راجع به شرایط انسانی نماییم که به سختی از موش می توان به دست آورد. “
مدل سازی میکروبیوم روده انسان
رشد باکتری های مرتبط با بیماری کرون در آزمایشگاه دشوار است، اما مهندسان MIT راهی برای آن پیدا کرده اند.
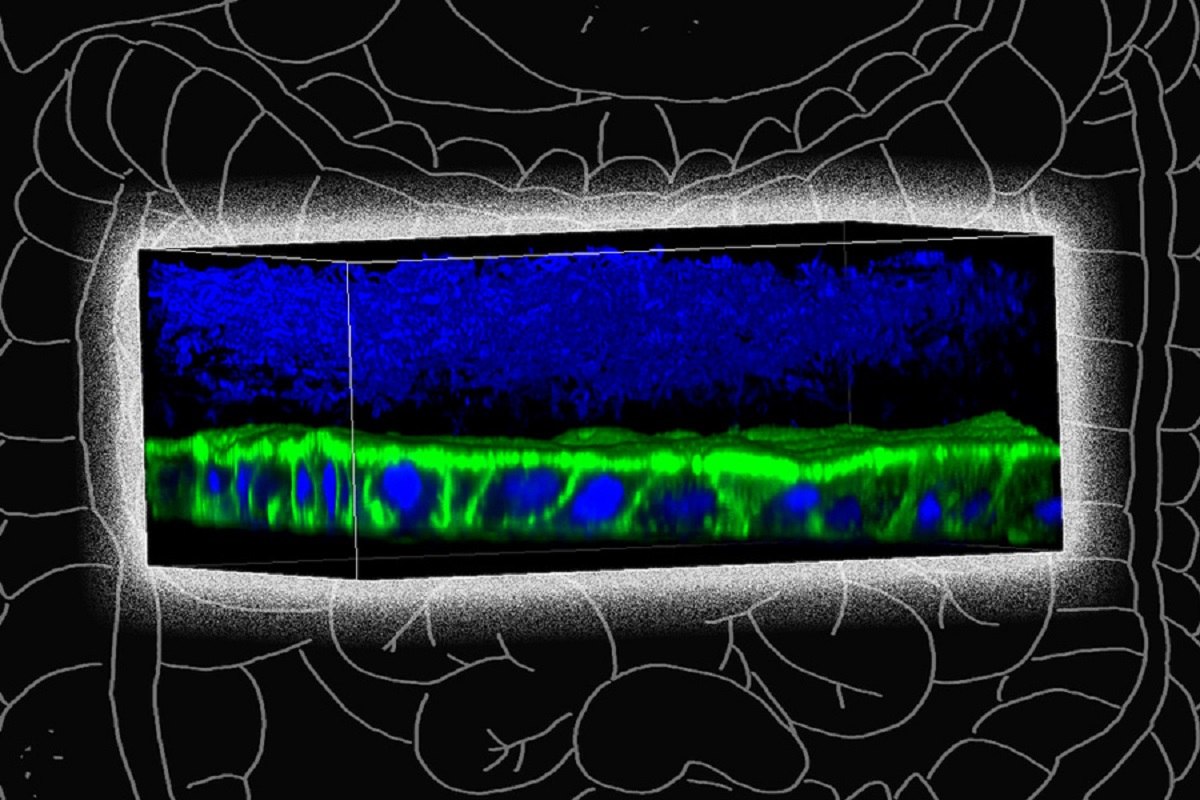
تصویر: مدل میکروبیوم. مهندسان بیولوژیک و مکانیک MIT دستگاه ویژه ای را طراحی کرده اند که در آن می توانند باکتری های نامقاوم در برابر اکسیژن را در بافت هایی که پوشش داخلی روده بزرگ را تکثیر می کنند، رشد دهند. باکتری F. prausnitzii (آبی ، در بالای تصویر) در بالای لایه ای از سلول های سد مخاط انسان (سبز و آبی) رشد می کند. جیانبو ژانگ. پس زمینه ویرایش شده توسط اخبار MIT
چندین هزار سویه باکتری در روده انسان زندگی می کنند. برخی از آنها با بیماری در ارتباط هستند، در حالی که برخی دیگر اثرات مفیدی بر سلامت انسان دارند. کشف نقش دقیق هر یک از این باکتری ها می تواند دشوار باشد، زیرا بسیاری از آنها را نمی توان در مطالعات آزمایشگاهی با استفاده از بافت انسان رشد داد.
این دشواری به ویژه برای گونه هایی که نمی توانند در محیط های غنی از اکسیژن زندگی کنند، بارزتر است. با این حال، مهندسان بیولوژیک و مکانیک MIT در حال حاضر دستگاه ویژه ای را طراحی کرده اند که در آن می توانند آن باکتری های نامقاوم در برابر اکسیژن را در بافت رشد دهند که آستر یا پوشش داخلی روده بزرگ را تکثیر می کنند، و این دستگاه به آنها اجازه می دهد تا چهار روز زنده بمانند.
با استفاده از این سیستم، محققان نشان دادند که می توانند یک سویه باکتری به نام Faecalibacterium prausnitzii را رشد دهند که در روده انسان زندگی می کند و در مقابل التهاب از ما محافظت می کند.لیندا گریفیت، استاد دانشکده مهندسی آموزش نو آوری در گروه مهندسی بیولوژی MIT می گوید: “ما فکر کردیم که واقعاً مشارکت در ساخت ابزاری برای جامعه که می تواند در این موارد شدید مورد استفاده قرار گیرد بسیار مهم است.” “ما نشان دادیم که شما می توانید این ارگانیسم های بسیار سریع را رشد دهید، و ما توانستیم تأثیرات آنها را بر روی روده بزرگ انسان بررسی کنیم. “
با استفاده از این سیستم، محققان نشان دادند که می توانند یک سویه باکتری به نام Faecalibacterium prausnitzii را رشد دهند که در روده انسان زندگی می کند و در مقابل التهاب از ما محافظت می کند. آنها همچنین نشان دادند که این باکتری ها، که اغلب در بیماران مبتلا به بیماری کرون کاهش می یابند، به نظر می رسد بسیاری از اثرات محافظتی خود را از طریق ترشح یک اسید چرب به نام بوتیرات اعمال می کنند.
حساسیت به اکسیژن
گریفیت می گوید، مدل کردن محیط میکروبیوم پیچیده روده انسان با استفاده از حیواناتی مانند موش دشوار است، تا حدی به این دلیل که موش ها رژیم غذایی بسیار متفاوتی از انسان دارند.
او می گوید: “ما مطالب زیادی از موش ها و سایر مدل های حیوانی آموخته ایم، اما تفاوت های زیادی وجود دارد، خصوصاً در مورد میکروبیوم روده. “
بیشتر باکتری هایی که در روده انسان زندگی می کنند بی هوازی هستند، به این معنی که برای زنده ماندن به اکسیژن نیاز ندارند. برخی از این باکتری ها می توانند سطح پایینی از اکسیژن را تحمل کنند، در حالی که برخی دیگر مانند F. prausnitzii نمی توانند در معرض اکسیژن زنده بمانند، که این امر، مطالعه آنها را در آزمایشگاه دشوار می کند. برخی از محققان دستگاه هایی را طراحی کرده اند که در آن می توانند سلول های روده بزرگ انسان را به همراه باکتری هایی که سطح پایینی از اکسیژن را تحمل می کنند رشد دهند، اما این موارد برای F. prausnitzii و سایر میکروب های بسیار نامقاوم در برابر اکسیژن خوب کار نمی کنند.
برای غلبه بر این مشکل، تیم MIT دستگاهی را طراحی کرد که به آنها امکان می دهد سطح اکسیژن را در هر قسمت از سیستم دقیقاً کنترل کنند. دستگاه آنها حاوی کانالی است که از سلول های سد مخاطی روده بزرگ انسان پوشانده شده است. در زیر این سلول ها مواد مغذی برای زنده نگه داشتن سلول ها پمپ می شود. این لایه پایین غنی از اکسیژن است، اما غلظت اکسیژن به سمت بالای لایه سلول مخاطی کاهش می یابد، همان چیزی که در قسمت داخلی روده بزرگ انسان اتفاق می افتد.
همان طور که در روده بزرگ انسان انجام می شود، سلول های سد در کانال یک لایه متراکم از مخاط ترشح می کنند. تیم MIT نشان داد که F. prausnitzii می تواند در لایه بیرونی این مخاط ابرهایی از سلول ها تشکیل دهد و تا چهار روز در آن جا زنده بماند، یعنی در محیطی که توسط مایعاتی که از آن عبور می کند بدون اکسیژن نگهداری می شود. این مایع همچنین حاوی مواد مغذی برای میکروب ها است.
با استفاده از این سیستم، محققان توانستند نشان دهند که F. prausnitzii بر روی مسیرهای سلولی درگیر در التهاب تأثیر می گذارد. آنها مشاهده کردند که این باکتری ها یک اسید چرب کوتاه زنجیره ای به نام بوتیرات تولید می کنند که قبلاً نشان داده شده است که التهاب را کاهش می دهد. پس از بالا رفتن سطح بوتیرات، سلول های مخاطی کاهش فعالیت در مسیری به نام NF kappa B را نشان دادند. این کاهش باعث آرام شدن التهاب می شود.
چندین هزار سویه باکتری در روده انسان زندگی می کنند. برخی از آنها با بیماری در ارتباط هستند، در حالی که برخی دیگر اثرات مفیدی بر سلامت انسان دارند. ژانگ می گوید: “به طور کلی، این مسیر کاهش یافته است که واقعاً شبیه آن چیزی است که مردم در انسان دیده اند.” “به نظر می رسد که باکتری ها در حال حساسیت زدایی از سلول های پستانداران هستند تا آنها در مقابل خطرات موجود در محیط بیرونی واکنش زیادی نشان ندهند، و بنابراین توسط باکتری ها حالت التهاب در حال آرام شدن است. “
بیماران مبتلا به بیماری کرون اغلب سطح F. prausnitzii را کاهش می دهند و فرض می شود که نبود آن باکتری ها در التهاب بیش فعالی دیده شده در آن بیماران نقش دارد.
هنگامی که محققان بوتیرات را به سیستم اضافه کردند، بدون باکتری، این همه اثراتی را که آنها هنگام حضور باکتری مشاهده کردند، ایجاد نکرد. این نشان می دهد که برخی از اثرات باکتری ممکن است از طریق مکانیسم های دیگری اعمال شود، که محققان امیدوارند بتوانند در این مورد بیشتر بررسی کنند.
میکروب ها و بیماری ها
محققان همچنین قصد دارند با استفاده از سیستم خود بررسی کنند که، هنگامی که آنها گونه های دیگری از باکتری را که اعتقاد دارند در بیماری کرون نقش دارند اضافه می کنند تا بتوانند اثرات هر گونه را بیشتر کشف کنند، چه اتفاقی می افتد.
آنها همچنین در حال برنامه ریزی برای مطالعه و همکاری با آلسیو فاسانو، رئیس بخش گوارش و تغذیه کودکان در بیمارستان عمومی ماساچوست، برای رشد بافت مخاطی بیماران مبتلا به بیماری سلیاک و سایر اختلالات دستگاه گوارش هستند. سپس می توان از این بافت برای مطالعه التهاب ناشی از میکروب در سلول هایی با زمینه های مختلف ژنتیکی استفاده کرد.
گریفیت می گوید، “ما امیدواریم که داده های جدیدی به دست آوریم که نشان می دهد چگونه میکروب ها و التهاب با زمینه ژنتیکی میزبان کار می کنند، تا ببینیم آیا افرادی می توانند استعداد ژنتیکی داشته باشند که میکروب ها کمی بیشتر با سد مخاطی آنها تداخل داشته باشند.”

تصویر: مدل میکروبیوم. این عکس، شماتیک دستگاه جدیدی را نشان می دهد که مهندسان MIT ساخته اند که به آنها امکان می دهد تا بافت روده بزرگ انسان را همراه با باکتری های نامقاوم در برابر اکسیژن که به طور معمول در دستگاه گوارش انسان زندگی می کنند، رشد دهند. جیانبو ژانگ
مغز تعاملات زیادی با دستگاه گوارش دارد که این تعاملات می تواند از طریق سیستم عصبی روده یا از طریق گردش سلول های ایمنی، مواد مغذی و هورمون ها بین اندام ها، باشد. وی همچنین امیدوار است که از این دستگاه برای بررسی سایر موانع مخاطی، از جمله در دستگاه تولید مثل زنان، مانند دهانه رحم و آندومتر، استفاده کند.
بودجه این تحقیق توسط موسسه ملی بهداشت ایالات متحده ، برنامه Boehringer Ingelheim SHINE و انستیتوی ملی علوم بهداشت محیط تأمین شد.
منبع: آن ترافتون، دفتر خبری MIT
 قوی ترین طلسمات+قویترین دعا و طلسم+قوی ترین کتاب طلسم و دعانویسی مطالب مذهبی+طلسم سیاهی و طلاق+طلسم احضار محبت معشوق+دانلود کتاب طلسم محبت و طلاق قوی
قوی ترین طلسمات+قویترین دعا و طلسم+قوی ترین کتاب طلسم و دعانویسی مطالب مذهبی+طلسم سیاهی و طلاق+طلسم احضار محبت معشوق+دانلود کتاب طلسم محبت و طلاق قوی